背景と目的
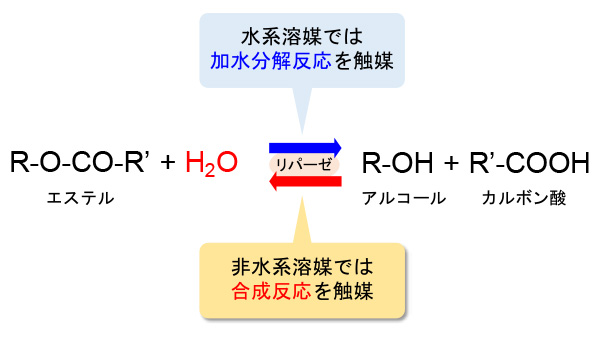
酵素は、主にタンパク質からなる高分子化合物であり、生物体内で起こる様々な消化反応や物質変換反応に対して触媒作用を示す。酵素反応は、生体内の各種成分に対して特異的かつ選択的な触媒作用を示し、かつ常温・常圧下で効率良く反応が進行するといった特徴をもつ。通常、酵素は多くの水の存在下で起こる水系反応を触媒する。たとえば、脂質加水分解酵素として知られるリパーゼは、水系では油脂をはじめとするエステルの加水分解を触媒する。しかし、水が極端に少ない環境下では、加水分解の逆反応、すなわち脱水縮合によりエステルと水を生成する反応に対して触媒作用を示す(図1)。酵素反応のこのような特徴と、反応物に対する高度な選択性、生体適合性、環境適合性を活かして、バイオディーゼル燃料や医薬、化粧品、食品などの分野でリパーゼを用いた非水系酵素反応による有機合成法が注目されている1, 2)。しかし、非水溶媒中でのリパーゼの利用にあたっては、アルカリ触媒などの無機触媒と比較して反応速度が遅いことが問題となっており、非水系酵素反応の速度向上が求められている。
本研究では、有機溶媒中に分散させたリパーゼ粉末に少量の水を添加して水和・凝集状態にすると、触媒活性が飛躍的に向上する現象3)に注目し、新たなリパーゼの前処理方法として「水和凝集法」の開発を試みた。本法では、酵素活性向上のために特殊な化合物の添加や架橋などの化学処理を必要としないため、食品や医薬品を含む様々な分野で利用可能なリパーゼ触媒を開発できると期待される。
研究成果の概要
1. 水和凝集処理によるリパーゼの活性化
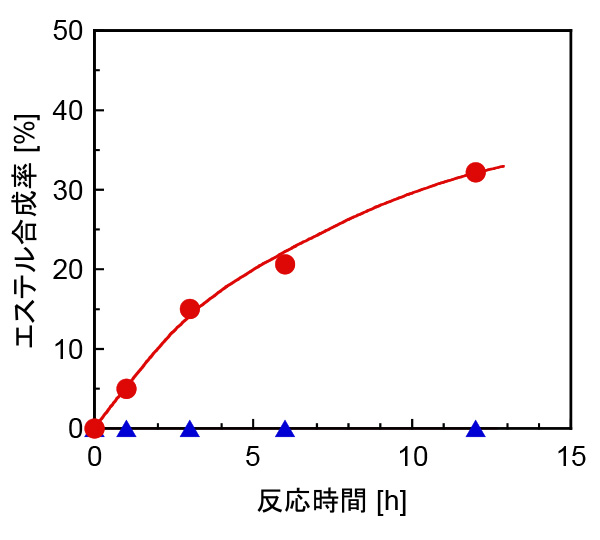
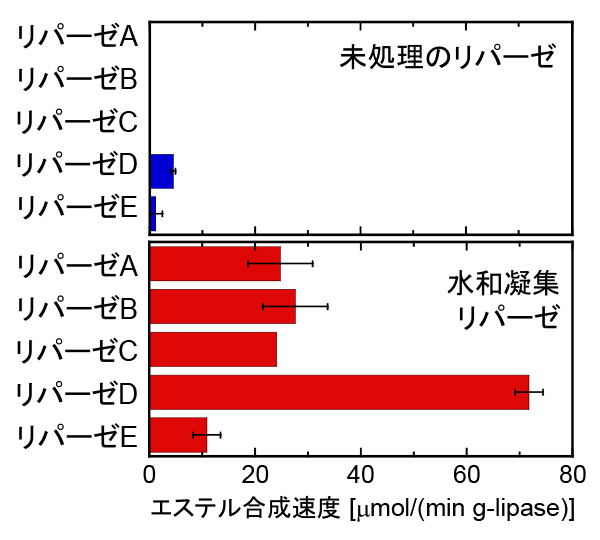
市販のリパーゼ粉末を直鎖アルコール中に分散させ、これに所定量の水溶液を滴下し、室温下で数時間撹拌すると、リパーゼが水和してペースト状の凝集物となった。その後、直鎖アルコール相を取り除き、ペースト状の残渣を凍結乾燥することで、水和凝集処理を施した「水和凝集リパーゼ」を作製した。長鎖脂肪酸とメタノールを原料として脂肪酸メチルエステル合成速度を調べたところ、未処理のリパーゼではエステルの合成が認められなかったのに対し、水和凝集リパーゼではエステル合成の進行が認められ、顕著な活性化効果が示された(図2)。さらに、カビ類(リパーゼA, D)、バクテリア類(リパーゼB, E)、哺乳類(リパーゼC)に由来する様々なリパーゼに対して、水和凝集処理による反応速度の向上効果が認められ(図3)、水和凝集処理が様々なリパーゼの活性化に有効であることが明らかとなった。水和凝集リパーゼは、乾燥状態で1か月冷蔵保存した後にも作製直後と同様のエステル合成活性を示し、活性化後の保存が可能であることもわかった。
2. 水和凝集リパーゼの活性化メカニズム
続いて、分光学的手法により水和凝集処理による活性化メカニズムについて検討した。タンパク質の分子構造を反映する赤外吸収スペクトルおよび蛍光スペクトルを測定したところ、水和凝集処理の前後でリパーゼの分子構造が部分的に変化している可能性が示唆された。リパーゼは、水と油の境界(界面)に吸着することで活性な分子構造が変化し、この状態で高い酵素活性を発現することが知られている4)。顕微鏡観察の結果、水和凝集処理の過程で生成するペースト状の凝集物には直鎖アルコールと水との界面が多く存在していることがわかり、界面におけるリパーゼの分子構造の変化が反応速度の向上に寄与したと考えられる。
3. 水和凝集リパーゼの反応特性評価と様々なエステル合成への展開
水和凝集リパーゼを用いたエステル合成反応の特性について、酵素反応速度論的な見地から検討した。長鎖脂肪酸とアルコールを原料とする2基質反応をベースとした反応モデルを適用し、それぞれの原料に対する反応速度の濃度依存性を詳細に調べ、反応速度パラメーターを具体的に求めた。その結果、従来の活性化手法に匹敵する反応特性を有することが示された。さらに、反応速度の温度依存性も明らかにし、見かけの活性化エネルギーの値を求めることができた。本来、非水系溶媒中で極めて活性の低いリパーゼに対してこれらの反応速度パラメーターや活性化エネルギーに関する定量的なデータは非常に限られており、将来の反応プロセスの設計および制御に向けて有意義な成果が得られたといえる。
水和凝集リパーゼの有機合成分野への適用可能性を検証するため、種々の基質を用いたエステル合成反応についても検討した。脂肪酸の鎖長や飽和度、アルコール基質の分子サイズ、エステルを原料とした各種エステル交換反応などを行い、いずれにおいても未処理のリパーゼでは進行しない(またはきわめて反応速度が遅い)反応に対する活性化効果を確認した。
まとめと今後の展望
本研究では、新規なリパーゼの活性化手法として「水和凝集法」を提案し、その特徴について検討を行った。特殊な機器や試薬、高度な分子合成技術を用いることなく、簡便な手順でリパーゼの触媒活性を飛躍的に高めることに成功した。既往の方法では困難であった、非水溶媒中での酵素反応に関する基礎的データを得ることが可能であるばかりでなく、市販リパーゼの触媒活性を高めて有用物質の合成に適用できる可能性を示す有意義な成果が得られた。今後、水和凝集リパーゼの触媒活性に関する基盤的データを蓄積してその反応特性を詳細に解明し、有機合成用の新たな選択肢として水和凝集リパーゼの有用性を示していきたいと考えている。
参考文献
1) P. Adlercreutz: Chem. Soc. Rev., 42, 6406-6436 (2013).
2) J. K. Poppe et al.: Biotechnol. Adv., 33, 511-525 (2015).
3) T. Kuroiwa et al.: Process Biochem., 51, 2047-2054 (2016).
4) A. M. Brzozowski et al.: Nature, 351, 491-494 (1991).
研究成果
支援を受けたテーマに関連する成果
査読付き学術論文
1. Maho Katayama, Takashi Kuroiwa, Kenya Suzuno, Ayumi Igusa, Toru Matsui, Akihiko Kanazawa: Hydration-aggregation pretreatment for drastically improving esterification activity of commercial lipases in non-aqueous media. Enzyme Microb. Technol., 105, 30-37, 2017.
学会発表
1. Kohei Takeda, Takashi Kuroiwa, Yoshihiro Aoki, Akihiko Kanazawa: Enzymatic synthesis of trehalose esters via lipase-catalyzed transesterification using triacylgrycerols with different acyl groups. The 17th Congress of Asian Pacific Confederation of Chemical Engineering, Hong Kong Convention and Exhibition Center (Hong Kong, China), Nano-Mat-P8, p. 625, Aug. 2017.
2. 竹田昂平, 黒岩崇, 青木宜丈, 金澤昭彦:「リパーゼを触媒とするトレハロースのアシル化反応におけるアシル供与基質の影響」, 化学工学会第49回秋季大会, 名古屋大学(愛知県名古屋市), 講演要旨集PB224, 2017年9月.
3. 黒岩 崇, 片山真穂, 岡部徳文, 金澤昭彦: 「リパーゼを用いたエステル生成反応に対する水和凝集処理の活性向上効果」, 日本食品工学会第18回(2017年度)年次大会, 関西大学(大阪府吹田市), 講演要旨集p. 46, 2017年8月.
4. 竹田昂平, 黒岩 崇, 青木宜丈, 金澤昭彦:「トリグリセリド基質を用いたトレハロースの酵素的アシル化における構成脂肪酸の影響」, 日本食品工学会第18回(2017年度)年次大会, 関西大学(大阪府吹田市), 講演要旨集p. 109, 2017年8月.
その他のテーマに関連する研究成果(件数のみ)
・著書1件(2018年8月出版予定)
・査読付き学術論文3件
・国際学会発表1件
・国内学会発表8件(うち招待講演2件)
・学会等からの受賞2件